Тысячи спасенных жизней начинаются с одной молекулы.
Первый разработанный в РФ истинный противовирусный препарат для лечения вируса инфекционного перитонита кошек (ИПК/FIP) Ипекон® успешно прошел клинические испытания.
В феврале 2024 года успешно завершились официальные зарегистрированные мультицентровые рандомизированные сравнительные клинические исследования нового препарата для лечения инфекционного перитонита кошек «Ипекон®».
А уже в июне 2024 года ветеринарная компания ООО «ВЕТСТЕМ» - резидент Сколково, заявила о получении официальной регистрации первого российского истинного противовирусного препарата «Ипекон®». Номер РУ 77-3-11.24-5173№ПВР-3-11.24/03980
Клинические исследования препарата проводились в трех крупнейших ветеринарных клиниках г. Москвы: «Центр ветеринарной медицины «АВВЕТУРА»», сеть ветеринарных клиник «Триовет», ветеринарная клиника «Кибелла».
В испытании приняли участие 38 кошек от 6 месяцев до 2,5 лет. Из них 18 животных экссудативной и 20 с не экссудативной («сухой») формой ИПК/FIP.
Животных включали по следующим критериям:
Критериями исключения считались:
Для диагностики экссудативной формы инфекционного перитонита кошек использовали ПЦР выпотной жидкости и тест Ривальта (проба Ривальта). Для не экссудативной формы (неврологической, офтальмологической) применяли ПЦР материала, полученного при тонкоигольной аспирационной биопсии регионального лимфоузла.
Испытуемые животные были разделены на 3 группы: с экссудативной формой ИПК/FIP, которые получали Ипекон в дозе 8 мг/кг, с экссудативной формой ИПК/FIP в тяжелом состоянии или пациенты с не экссудативной («сухой») формой 10 мг/кг, с не экссудативной («сухой») формой ИПК/FIP 12мг/кг.
Раствор вводили подкожно ежедневно один раз в день с интервалом между инъекциями 24 часа в течение всего курса лечения.
Оценка эффективности лечения проводилась на основании анализа динамики общего клинического состояния
Результаты исследования
Общее клиническое состояние:
Оценка эффективности лечения
Динамика массы тела:
У всех животных проводимая терапия сопровождалась положительной динамикой массы тела. Уже после первых двух-трех недель терапии у большинства животных масса тела увеличилась на 100-200 г. Вес кошек на протяжении всего исследования постепенного возрастал до стабилизации согласно индивидуальным особенностям пациента (возраст, пол, порода).
Оценка эффективности лечения
Динамика общеклинических показателей крови:
Во всех трех группах у пациентов наблюдалась стабилизация клинических и биохимических показателей крови: снижение лейкоцитов, повышение гемоглобина, эритроцитов и гематокрита.
Первый разработанный в РФ истинный противовирусный препарат для лечения вируса инфекционного перитонита кошек (ИПК/FIP) Ипекон® успешно прошел клинические испытания.
В феврале 2024 года успешно завершились официальные зарегистрированные мультицентровые рандомизированные сравнительные клинические исследования нового препарата для лечения инфекционного перитонита кошек «Ипекон®».
А уже в июне 2024 года ветеринарная компания ООО «ВЕТСТЕМ» - резидент Сколково, заявила о получении официальной регистрации первого российского истинного противовирусного препарата «Ипекон®». Номер РУ 77-3-11.24-5173№ПВР-3-11.24/03980
Клинические исследования препарата проводились в трех крупнейших ветеринарных клиниках г. Москвы: «Центр ветеринарной медицины «АВВЕТУРА»», сеть ветеринарных клиник «Триовет», ветеринарная клиника «Кибелла».
В испытании приняли участие 38 кошек от 6 месяцев до 2,5 лет. Из них 18 животных экссудативной и 20 с не экссудативной («сухой») формой ИПК/FIP.
Животных включали по следующим критериям:
- клинические признаки ИПК/FIP;
- подтверждение диагноза ИПК/FIP;
- животные предварительно вакцинированы и прошли обработку от внутренних и внешних паразитов.
Критериями исключения считались:
- терминальное состояние пациента;
- признаки других заболеваний/патологий внутренних органов и систем в стадии декомпенсации;
- сопутствующие онкологические процессы;
- прием противовирусных лекарственных препаратов в течение последней недели;
- диагностированные сочетанные вирусные заболевания* (панлейкопения, иммунодефицит кошек, кальцивирусная инфекция, вирусная лейкемия кошек)
Для диагностики экссудативной формы инфекционного перитонита кошек использовали ПЦР выпотной жидкости и тест Ривальта (проба Ривальта). Для не экссудативной формы (неврологической, офтальмологической) применяли ПЦР материала, полученного при тонкоигольной аспирационной биопсии регионального лимфоузла.
Испытуемые животные были разделены на 3 группы: с экссудативной формой ИПК/FIP, которые получали Ипекон в дозе 8 мг/кг, с экссудативной формой ИПК/FIP в тяжелом состоянии или пациенты с не экссудативной («сухой») формой 10 мг/кг, с не экссудативной («сухой») формой ИПК/FIP 12мг/кг.
Раствор вводили подкожно ежедневно один раз в день с интервалом между инъекциями 24 часа в течение всего курса лечения.
Оценка эффективности лечения проводилась на основании анализа динамики общего клинического состояния
- массы тела
- температуры тела
- общеклинических показателей крови
- биохимических показателей крови
- ультразвуковых исследований
Результаты исследования
- На первичном приеме отмечены характерные клинические признаки ИПК/FIP: дегидратация, увеличение лимфоузлов, гипертермия, снижение или отсутствие аппетита, потеря веса и т.д.
- По результатам УЗИ – увеличение лимфоузлов, селезенки, пиогранулямотозные изменения внутренних органов, признаки диффузных изменений почек, признаки хронического энтерита/хронической энтеропатии; умеренного острого энтерита, гепатопатии, холангита. панкреатита. У пациентов с экссудативной формой в брюшной или плевральной полости определяли наличие выпотную жидкость.
- Данные общеклинического и биохимического исследований крови: лейкоцитоз или, критическую лейкопению), нейтрофилию, лимфоцитопению, эритроцитопению, низкий гематокрит (у преобладающего числа пациентов 12-24 %), тромбоцитопению, а также гипергаммаглобинемию, высокий уровень общего белка, повышение печеночных трансфераз, билирубина, щелочной фосфатазы.
Общее клиническое состояние:
- после начала терапии состояние было стабильным, прослеживалась положительная динамика: животные стали активнее, нормализовался аппетит, исчезли признаки дегидратации, видимые слизистые оболочки бледно-розового или розового цвета, температура тела в пределах физиологических границ для вида. Частота дефекации за первые две недели нормализовалась примерно у 90% животных с первоначальными нарушениями, а к концу первого месяца лечения – у всех. Улучшение общего состояния, нормализация работы ЖКТ сопровождались постепенным набором веса. У кота с тяжелыми неврологическими симптомами (судороги) при включении в исследование (в начале терапии) этот симптом больше не наблюдался.
- По результатам оценки слабой динамики лечения у пяти пациентов было принято решение о повышении дозы на 2 мг/кг. Предпринятые действия позволили стабилизировать состояние, купировать нежелательные симптомы и обеспечить положительную динамику.
Оценка эффективности лечения
Динамика массы тела:
У всех животных проводимая терапия сопровождалась положительной динамикой массы тела. Уже после первых двух-трех недель терапии у большинства животных масса тела увеличилась на 100-200 г. Вес кошек на протяжении всего исследования постепенного возрастал до стабилизации согласно индивидуальным особенностям пациента (возраст, пол, порода).
Оценка эффективности лечения
Динамика общеклинических показателей крови:
Во всех трех группах у пациентов наблюдалась стабилизация клинических и биохимических показателей крови: снижение лейкоцитов, повышение гемоглобина, эритроцитов и гематокрита.
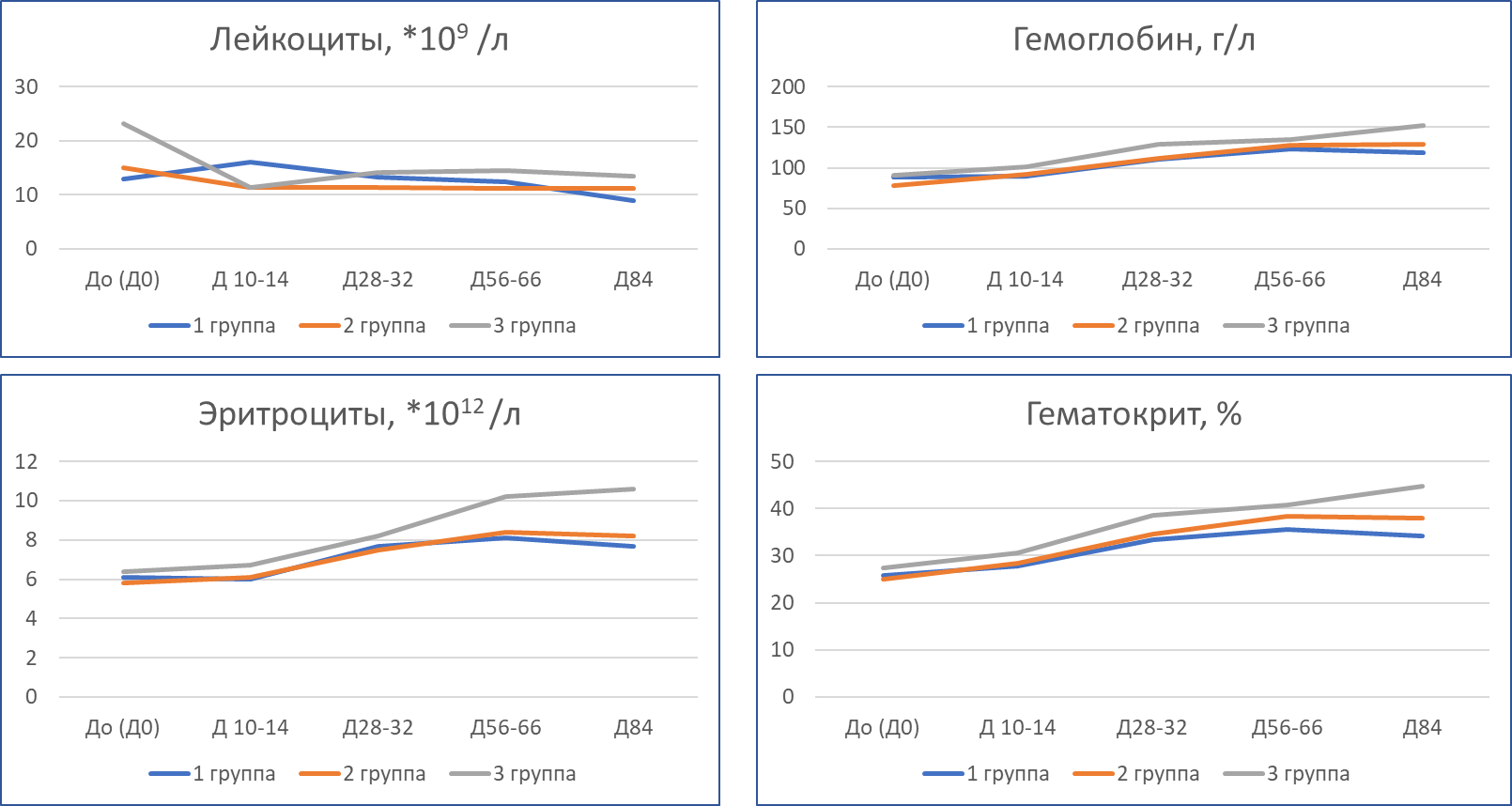
Динамика биохимических показателей крови:
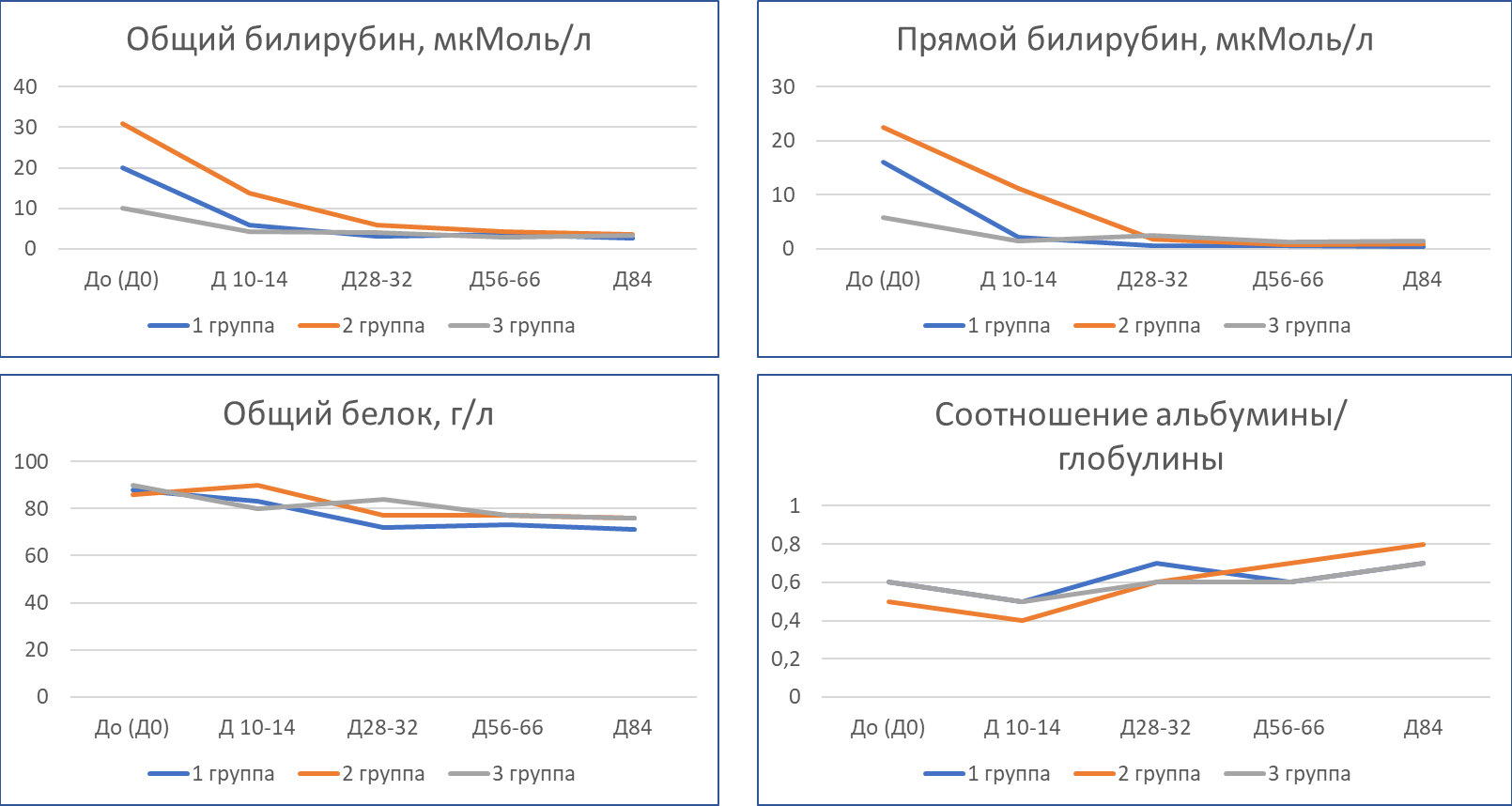
Результаты клинического исследования
24 пациента (85,7%) на момент окончания курса лечения (84 дня) имели статус «клиническое выздоровление», были активны, имели хороший аппетит, основные физиологические показатели - в пределах нормальных значений.
После завершения курса лечения препаратом Ипекон® все животных находились в стабильном состоянии, рецидивы не наблюдались, летальность отсутствовала. Период наблюдений составил около 2 месяцев.
Нежелательные явления/побочные эффекты
В ходе исследования был отмечен один случай нежелательной реакции, имеющий признаки аллергической. Данное явление разрешилось самостоятельно без дополнительной фармакотерапии в течении 2 дней.
Все животные испытывали дискомфорт и боль в момент введения препарата, однако проявляли индивидуальную чувствительность по-разному: некоторые «стойко» переносили инъекции, а другие сопровождали процедуру введения агрессивным поведением.
Других нежелательных реакций отмечено не было.
Местно-раздражающее действие
Только у 3 животных (10,7%) в местах введения препарата наблюдалась индивидуальная реакция в виде локального уплотнения подкожно-жировой клетчатки, абсцессы и повышения местной температуры.
Участки гиперчувствительности зажили самостоятельно без вспомогательного лекарственного воздействия.
Выводы:
24 пациента (85,7%) на момент окончания курса лечения (84 дня) имели статус «клиническое выздоровление», были активны, имели хороший аппетит, основные физиологические показатели - в пределах нормальных значений.
После завершения курса лечения препаратом Ипекон® все животных находились в стабильном состоянии, рецидивы не наблюдались, летальность отсутствовала. Период наблюдений составил около 2 месяцев.
Нежелательные явления/побочные эффекты
В ходе исследования был отмечен один случай нежелательной реакции, имеющий признаки аллергической. Данное явление разрешилось самостоятельно без дополнительной фармакотерапии в течении 2 дней.
Все животные испытывали дискомфорт и боль в момент введения препарата, однако проявляли индивидуальную чувствительность по-разному: некоторые «стойко» переносили инъекции, а другие сопровождали процедуру введения агрессивным поведением.
Других нежелательных реакций отмечено не было.
Местно-раздражающее действие
Только у 3 животных (10,7%) в местах введения препарата наблюдалась индивидуальная реакция в виде локального уплотнения подкожно-жировой клетчатки, абсцессы и повышения местной температуры.
Участки гиперчувствительности зажили самостоятельно без вспомогательного лекарственного воздействия.
Выводы:
- Применение препарата Ипекон® при лечении вирусного перитонита кошек обеспечивает высокую терапевтическую эффективность: 85,7% пациентов по окончании курсового лечения имели статус «клиническое выздоровление»
- Переносимость препарата Ипекон® при многократном подкожном применении хорошая, присутствует дискомфорт при введении, однако признаков интоксикации или клинически выраженных отклонений, ухудшения функций органов и систем не выявлено
- Во время применения препарата Ипекон® отмечен только один случай нежелательной реакции, имеющей признаки аллергической.
- Рецидивов клинической манифестации ИПК/FIP после окончания курса препарата Ипекон® не выявлено.
